公共服务 |
||||||||||||||||||||||
|
||||||||||||||||||||||
cro服务 |
||||||||||||||||||
|
||||||||||||||||||
|
||
|
在现代生物学和生物医学研究中,临床试验日益成为从实验室研究到临床转变过程中 “必须经过的点”。伴随全球范围大幅增加的临床试验,伦理学问题也不断出现, 这些问题包括:治疗误解以及知情同意面临着的挑战;研究人员和临床工作者间的利益冲突;涉及人类受试者的研究相关的问题和利益分享问题;临床试验中的公平和随访问题;在临床试验中使用安慰剂的伦理问题等;临床试验的核心是否经得起科学的考验以及整个过程是否符合伦理。所以伦理审查在保护受试者权利、安全和福利的同时,也是保证临床试验经得起考验的关键环节。在遵循公正、独立、多元、透明和不营利的原则下,上海医药临床研究中心伦理委员会提供以下服务: (1)提供独立的伦理审查
四类伦理审查项目所需提交的材料清单 表格下载 联系ag凯发旗舰厅 |
||
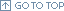 |